En bref
En 2017, la France était au 6e rang des pays les plus consommateurs d’antibiotiques dans le secteur de ville en Europe. L’antibiorésistance est la cause de 5 543 décès par an chez des patients atteints d’infections à Bactéries Résistantes. Face à ce phénomène mondial, l’Organisation mondiale de la santé, l’Union européenne, la France se sont engagées dans des programmes de prévention de l’antibiorésistance. Plus près de vous, votre URPS des chirurgiens-dentistes d’Île-de-France avec l’URPS des Hauts de France avont également déployé dernièrement plusieurs projets. L’antibiorésistance, la définir, connaître ses causes, ses conséquences, comment lutter contre celle-ci… Autant de questions auxquelles nous apportons des réponses dans ce dossier.
C’est en 1928 qu’était découverte, un peu par hasard, la pénicilline. Cette substance était capable d’inhiber la prolifération d’un grand nombre de bactéries courantes. Pendant la seconde guerre mondiale son usage clinique fût développé. L’antibiotique était né. Sa production et son utilisation à grande échelle allaient débuter après la seconde guerre mondiale. Cette découverte constituât une percée médicale majeure qui allait entrainer au moins dix ans de gain d’espérance de vie permettant de traiter avec succès nombre de maladies jusque-là mortelles. Cette efficacité a motivé un usage des antibiotiques de plus en plus fréquent et parfois injustifié (choix des molécules, durées ou posologie des traitements inadaptés, mauvaise observance), tant chez l’homme qu’en médecine vétérinaire où il a favorisé l’apparition de bactéries résistantes à ces traitements. Résultat, aujourd’hui, la résistance bactérienne est devenue un phénomène global et préoccupant. Un problème de santé publique mondial. Le paradoxe étant que tout le monde a conscience de l’existence du problème mais que les comportements peinent à évoluer pour s’engager durablement dans un cercle vertueux.
L’ANTIBIORESISTANCE, QU’EST-CE QUE C’EST ?
L’antibiorésistance est le phénomène qui consiste, pour une bactérie, à devenir résistante aux antibiotiques. Pendant longtemps, la majorité des cas de résistance était détectée à l’hôpital. Le phénomène prend de plus en plus d’ampleur en ville, au détour d’antibiothérapies apparemment anodines. Cette résistance peut être :
- Naturelle : une bactérie est insensible naturellement à certains antibiotiques,
- Acquise : une bactérie, auparavant sensible à un antibiotique, devient résistante.
LES CAUSES DE L’ANTIBIORESISTANCE
L’efficacité remarquable des antibiotiques a motivé leur utilisation massive et répétée en santé humaine et animale.
Or, le fait d’avoir utilisé de manière très importante des antibiotiques en santé humaine et animale est responsable de l’augmentation des résistances bactériennes aux antibiotiques.
Cette consommation peut avoir une origine environnementale. Elle sera imperceptible, involontaire et finalement subie.
En effet les bactéries multi-résistantes issues des élevages animaux peuvent se transmettre à l’être humain directement ou par la chaîne alimentaire. Ces bactéries résistantes sont également présentes dans les cours d’eau, en aval des villes ou des élevages, voire dans les nappes phréatiques.
La présence d’antibiotiques dans l’environnement ou de leurs produits de dégradation, en provenance de l’industrie, des hôpitaux, des eaux usées, des élevages, des abattoirs…, exerce une pression de sélection sur les bactéries, favorisant la persistance de bactéries multirésistantes.
Mais la consommation d’antibiotiques par l’homme demeure la source majeure d’ingestion. C’est son usage inadapté qui constitue l’une des causes de l’antibiorésistance.
Rappelons-le, les antibiotiques ne sont efficaces que sur les infections bactériennes. Ils n’ont aucun effet sur les virus et les champignons. Pourtant, à titre d’exemple, ils sont encore trop souvent prescrits pour des infections virales comme la grippe.
FOCUS COVID-19
Le Conseil national de l’Ordre des chirurgiens-dentistes, faisant suite aux publications du Haut conseil de la santé publique indique que de manière générale, il n’y a pas d’indication à prescrire une antibiothérapie dans les cas suivante :
- chez un patient présentant des symptômes rattachés à la Covid-19 confirmée (en dehors d’un autre foyer infectieux) du fait du caractère exceptionnel de la co-infection bactérienne ;
- en ville chez un patient ayant une infection respiratoire (haute ou basse) fortement évocatrice de Covid19 ou confirmée au SARS -CoV-2 ;
- en secteur d’hospitalisation, en l’absence de critère de gravité, dans l’attente des résultats microbiologiques et radiographiques, en hospitalisation conventionnelle où le patient peut être surveillé. Il n’y a pas non plus d’indication à initier ou poursuivre une antibiothérapie en cas de diagnostic de Covid-19 confirmé, si les symptômes cliniques et scanno-graphiques s’intègrent dans le tableau de Covid-19.
L’actualité concernant les traitements précoces de la Covid-19 ont mentionné l’usage de l’azithromycine (le coronavirus étant un virus à mécanisme d’infection intracellulaire, cet antibiotique pourrait interagir avec le virus et diminuer la gravité et la durée des symptômes), or, le Haut Conseil de la santé publique précise que dans l’infection par le SARS-CoV-2, la littérature n’apporte pas d’argument pour proposer la prescription d’azithromycine.
Contre la Covid-19, cette molécule a été évoquée dans le cadre du protocole de l’Institut HospitaloUniversitaire de Marseille. Pourtant, les récentes études publiées démontrent une inefficacité sur la mortalité à 28 jours et des effets secondaires notables (antibiorésistance accrue mais aussi aspergillose pulmonaire).
Ainsi, l’administration répétée d’antibiotiques chez l’homme ou l’animal est responsable de l’augmentation des résistances bactériennes aux antibiotiques en créant ce qu’on appelle une “pression de sélection” : le niveau d’antibiotique dans l’organisme atteint favorise les mutations et les échanges plasmidiques responsables d’acquisition de résistances aux antibiotiques. Ce phénomène tend à éliminer les bactéries sensibles pour laisser place aux bactéries résistantes. Plus on prend d’antibiotiques, plus le risque de faire émerger des bactéries résistantes s’accroît. Ces dernières rendent les traitements antibiotiques ultérieurs moins efficaces pour le patient.
La mauvaise utilisation des antibiotiques (traitements trop courts, trop longs ou à posologies inadaptées) peut également être pointée du doigt comme source de l’augmentation de l’antibiorésistance.
LES CONSEQUENCES DE L’ANTIBIORESISTANCE
Ces résistances aux antibiotiques sont devenues massives et préoccupantes. C’est ainsi que certaines souches sont multirésistantes, c’est-à-dire résistantes à plusieurs antibiotiques. D’autres sont même devenues toto-résistantes, c’est-à-dire résistantes à quasiment tous les antibiotiques disponibles. Ce phénomène, en augmentation constante, peut placer les prescripteurs dans une impasse thérapeutique.
On trouve des bactéries devenues résistantes aux antibiotiques dans la plupart des infections comme par exemple, les infections de la peau, des méningites, les infections sexuellement transmissibles, les infections urinaires ou les infections des voies respiratoires comme des pneumonies. Le traitement devient plus difficile, voire impossible parfois, du fait de la perte d’efficacité des antibiotiques.
Les conséquences se manifestent par le fait que :
- Le prescripteur a alors des difficultés à trouver un antibiotique efficace contre la bactérie en cause dans la maladie, ce qui se traduit par des symptômes qui durent plus longtemps, une aggravation de l’infection, des rechutes, des consultations répétées chez le médecin et par conséquence un temps de traitement allongé, une utilisation de médicaments plus puissants et plus chers pour arriver à soigner ;
- Les hospitalisations sont plus fréquentes et plus prolongées ;
- Les risques sont plus élevés lors d’interventions médicales, pour lesquelles les antibiotiques sont indispensables pour réduire les risques infectieux ;
- L’antibiorésistance bactérienne est une cause de mortalité, particulièrement chez les personnes fragiles : personnes âgées, nouveau-nés, femmes enceintes, personnes immunodéprimées, atteintes d’une maladie chronique ou hospitalisées. La résistance aux antibiotiques entraîne une augmentation des dépenses médicales, une prolongation des hospitalisations et une hausse de la mortalité.
La résistance aux antibiotiques entraîne une augmentation des dépenses médicales, une prolongation des hospitalisations et une hausse de la mortalité.
COMMENT LUTTER CONTRE L’ANTIBIORESISTANCE ?
PREVENIR LES INFECTIONS
Éviter la survenue des infections est la première étape de la lutte contre l’antibiorésistance. En effet, si les infections sont moins nombreuses, le recours aux antibiotiques sera moins fréquent. Pour prévenir les infections dans la vie quotidienne, les documents à destination du grand public rappellent les bases de l’hygiène :
- Se laver fréquemment les mains, surtout après un passage aux toilettes, au retour du travail à votre domicile, avant de préparer un repas, après avoir éternué et vous être mouché, avant et après avoir pris soin d’une personne, avant et après avoir pris soin de votre animal ;
- Conserver les aliments et préparer les repas dans les conditions adaptées pour chaque aliment (les garder propres, séparer les aliments crus et cuits, bien les cuire, les conserver aliments à une température adaptée) et choisir des aliments, notamment les produits d’élevage sans antibiotiques ;
- Respecter les vaccinations obligatoires et conseillées : elles vous protègent, vous et votre entourage. Certaines maladies bactériennes sont prévenues grâce à la vaccination (par exemple, contre lacoqueluche, contre certains germes responsables de pneumonies ou méningites : le pneumocoque, le méningocoque.
MIEUX UTILISER LES ANTIBIOTIQUES
En France, 93 % des antibiotiques sont utilisés en médecine de ville et 7 % en établissement de santé.
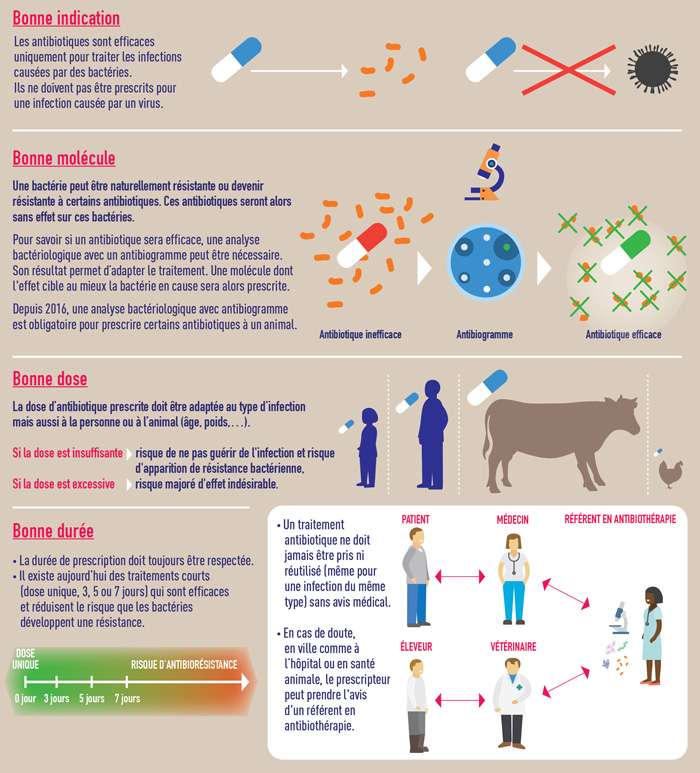
Pour que les antibiotiques restent efficaces, c’est-à-dire pour limiter l’apparition de bactéries résistantes, quelques principes d’utilisation sont de mise : la bonne molécule, à la bonne dose, et pour la bonne durée. Il existe également des tests de diagnostic rapides qui permettent d’aider au diagnostic d’une infection bactérienne et éviter des traitements antibiotiques inutiles (si les tests diagnostiques sont négatifs.
Soyons encore plus précis pour les prescripteurs et les usagers/consommateurs :
COTE PRESCRIPTEUR :
Il est important que les prescripteurs puissent :
- Distinguer les infections virales des infections bactériennes car les antibiotiques n’affectent pas les virus ;
- Choisir un antibiotique pertinent : en cas d’infection bactérienne, mieux vaut éviter l’utilisation systématique d’antibiotiques précieux (récents ou à large spectre) lorsque d’autres plus courants, ou à spectre plus étroit, suffisent et sont aussi efficaces. Le prescripteur doit pour cela savoir à quelles molécules réagit la bactérie responsable de la maladie de son patient. Il existe déjà des tests rapides de détection de la résistance à certains antibiotiques ; – Adapter la cure aux besoins, en particulier limiter la durée des traitements au strict nécessaire. Plus largement, pour prévenir et combattre la propagation de la résistance aux antibiotiques, les professionnels de santé peuvent :
- Faire de la prévention en veillant à la propreté des mains, des instruments et de leur environnement ;
- Ne prescrire et délivrer des antibiotiques que quand ils sont nécessaires, en application des directives en vigueur;
- Signaler les infections résistantes aux antibiotiques aux équipes de surveillance; – parler à leurs patients de la prise correcte des antibiotiques, des résistances et des dangers d’un usage abusif;
- Parler à leurs patients de la prévention des infections (par exemple, par la vaccination, le lavage des mains, les rapports sexuels à moindre risque ou en se couvrant la bouche et le nez pour éternuer).
COTE USAGER/CONSOMMATEUR :
Il est impératif que le patient envisage différemment la maladie et la façon de la soigner. Les campagnes de sensibilisation destinées à responsabiliser les usagers du système de santé en matière de consommation d’antibiotiques sont des outils pédagogiques nécessaires et utiles. Les habitudes sont difficiles à changer. La prescription d’antibiotiques est culturelle en France. Encore trop souvent un patient ne s’estime pas soigné s’il repart de chez son médecin sans ordonnance prescrivant un antibiotique.
Le patient doit en retenir les principes suivants :
- il ne doit pas avoir une consommation d’antibiotiques par habitude ;
- une prescription d’antibiotiques n’est pas une fin en soi ;
- il ne doit jamais exiger d’antibiotiques si le professionnel de santé déclare qu’il n’y a pas d’utilité à en prescrire.
Le patient doit faire confiance à son prescripteur qui sait quand les antibiotiques sont nécessaires et quand ils ne le sont pas.
Lorsqu’un traitement par antibiotiques est prescrit, le patient doit veiller à :
- bien respecter la dose, la fréquence des prises et la durée du traitement antibiotique prescrit;
- ne pas utiliser le traitement pour quelqu’un d’autre ou les traitements qui lui restent. Un traitement est spécifiquement prescrit pour un type d’infection bactérienne et adapté à chaque personne ;
- demander conseil au prescripteur en cas d’effet indésirable au traitement (éruption, nausées…) ;
- ne pas arrêter le traitement prématurément, même si l’état s’améliore. L’antibiotique doit être pris pendant la durée prescrite ;
- ne pas allonger de sa propre initiative la durée du traitement antibiotique, mais consulter son prescripteur si l’infection ne paraît pas guérie à la fin du traitement ;
- une fois le traitement terminé, ne pas réutiliser ultérieurement un antibiotique, même si le patient présente des symptômes qui ressemblent à ceux que le patient a eu antérieurement ;
- à la fin du traitement, rapporter au pharmacien toutes les boîtes entamées ou non utilisées.
L’ANTIBIORESISTANCE EN CHIFFRES
Selon une note de la Direction générale du Trésor Public, en 2016, la France était le 3ème pays européen dans lequel les antibiotiques étaient le plus prescrits après la Grèce et Chypre (données issues de l’European Centre for Disease Prevention and Control). En 2017, la France était au 6e rang des pays les plus consommateurs d’antibiotiques dans le secteur de ville en Europe, d’après les données du réseau européen ESAC-Net.
En 2019, il a été vendu en France :
- 772 tonnes d’antibiotiques destinés à la santé humaine.
- 422 tonnes d’antibiotiques destinés à la santé animale (96 % des antibiotiques sont administrés à des animaux destinés à la consommation humaine).
La consommation est passée entre 2009 et 2019 de 25,2 à 23,3 doses définies journalières (DDJ) pour 1 000 personnes et par jour (-7,4 %) Antibiotiques et résistance bactérienne : une infection virale respiratoire évitée, c’est un antibiotique préservé ! (santepubliquefrance.fr)
En France, l’antibiorésistance est la cause de 5 543 décès par an chez des patients atteints d’infections à Bactéries Résistantes A l’échelle mondiale, les résistances microbiennes seraient responsables de 700 000 morts par an. Si rien ne change, les maladies infectieuses d’origine bactériennes pourraient redevenir en 2050 une des premières causes de mortalité dans le monde, en provoquant jusqu’à 10 millions de morts.
Pour aller plus loin, vous trouverez ci-après un excellent document comportant de nombreuses cartes/infographies : SPF-AMR(v2)_29-05-18 (rencontressantepubliquefrance.fr)
LA LUTTE S’ORGANISE
Pour préserver le plus longtemps possible l’efficacité des antibiotiques disponibles, il est indispensable de réduire leur consommation afin de limiter la pression de sélection sur les bactéries.
Des campagnes de sensibilisation destinées à influencer et modifier le comportement du grand public ont fait baisser leur consommation qui reste cependant fluctuante. La France reste parmi les premiers utilisateurs mondiaux.Une utilisation raisonnée doit prévaloir.
Mais ce problème n’est pas seulement franco-français.
C’est pourquoi l’Union européenne a lancé des plans d’action en 2001, 2011 et 2017. Celui de 2017 prend en compte la dimension globale du problème et vise à faire du continent une région de pointe. Il comprend, entre autres, une action conjointe, la Joint Action on Antimicrobial Resistance & Healthcare – Associated Infections, coordonnée par l’Inserm. Elle rassemble 44 partenaires institutionnels – ministères de la Santé, instituts de recherche, instituts de santé publique – et vise à passer au concret, en particulier en s’inspirant de ce qui est déjà mis en place dans certains pays.
Plus largement, au niveau mondial, en mai 2015, l’OMS, la FAO (Food and Agriculture Organization, l’organisation des Nations unies pour l’alimentation et l’agriculture) et l’OIE (Office international des épizooties, devenu l’Organisation mondiale de la santé animale) ont adopté un Plan d’action mondial pour combattre la résistance aux antimicrobiens.
Il se décline en cinq axes :
- sensibiliser le personnel de santé et le public ;
- renforcer la surveillance et la recherche ;
- prendre des mesures d’assainissement, d’hygiène et de prévention des infections ;
- optimiser l’usage des antimicrobiens en santé humaine et animale ;
- soutenir des investissements durables pour la mise au point de nouveaux traitements, diagnostics ou vaccins.
